ASPEN: VALUTAZIONE DI ZANUBRUTINIB RISPETTO A IBRUTINIB
Studio ASPEN: valutazione di zanubrutinib rispetto a ibrutinib per la macroglobulinemia di Waldenström
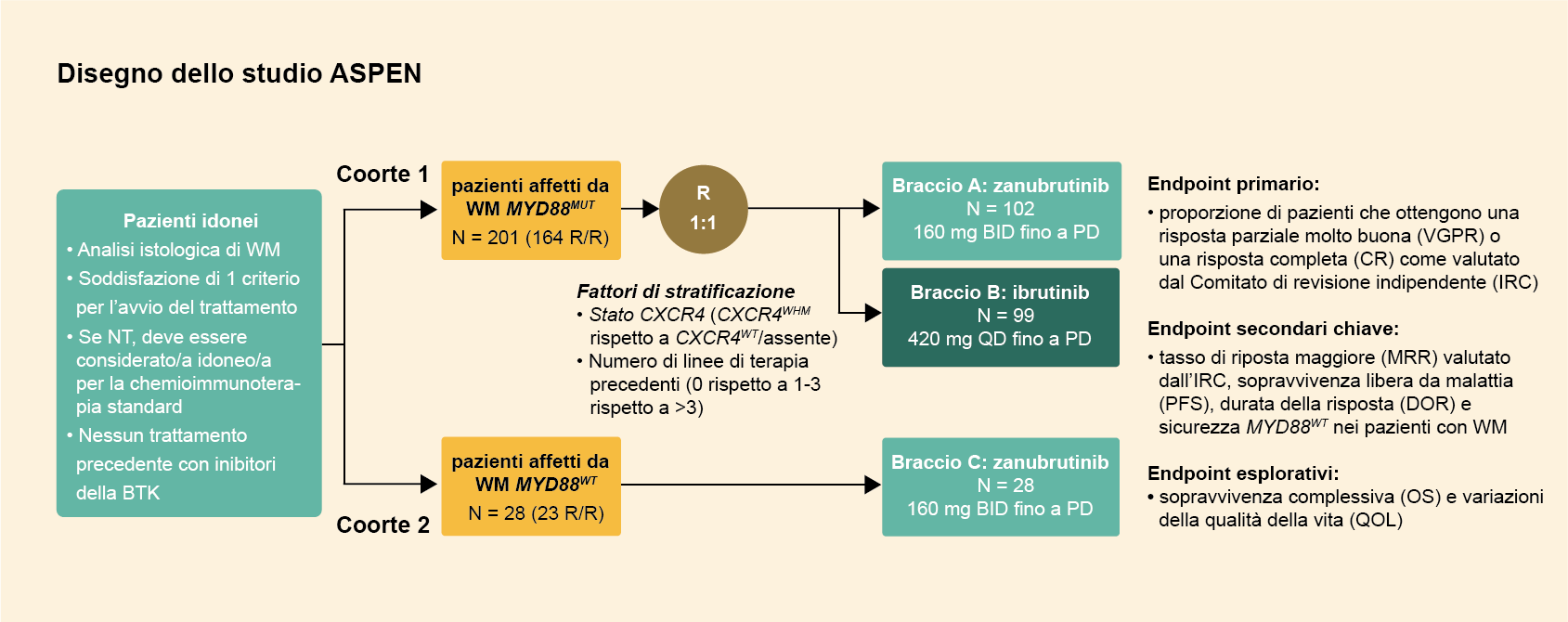
Disegno dello studio
Lo studio ASPEN ha randomizzato pazienti affetti da macroglobulinemia di Waldenström per ricevere ibrutinib oppure zanubrutinib e ha arruolato 229 pazienti (sia naïve al trattamento che con malattia recidivante o refrattaria)in 2 coorti: una coorte randomizzata (Coorte 1) che comprendeva 201 pazienti con una mutazione1 di MYD88 e una coorte non randomizzata (Coorte 2) con 28 pazienti affetti da malattia wild type/indeterminata.2
- I pazienti affetti da malattia con mutazione di MYD88L265P sono stati assegnati con un rapporto 1:1 a ibrutinib (420 mg una volta al giorno) o zanubrutinib (160 mg due volte al giorno), somministrati in cicli di 28 giorni fino alla progressione della malattia (PD) o fino allo sviluppo di intolleranza al trattamento (Coorte 1, N=201).1
- La maggior parte dei pazienti in entrambi i bracci soffriva di malattia recidivante/refrattaria (R/R; >80%), con una minoranza (<20%) naïve al trattamento (TN).(<20%).
- I fattori di stratificazione includevano stato di CXCR4 (CXCR4WHIM/CXCR4WT) e numero di linee di terapia precedenti (0, 1-3, o >3).
- I pazienti con malattia associata a MYD88 wild type ( MYD88WT )/stato di mutazione di MYD88 indeterminato hanno ricevuto zanubrutinib fino alla progressione della malattia all’interno di un terzo braccio non randomizzato (Coorte 2, N=28).2
Risultati: Coorte 1 (MYD88L265P)
Risposte
- Nessun paziente ha raggiunto una risposta completa (CR).
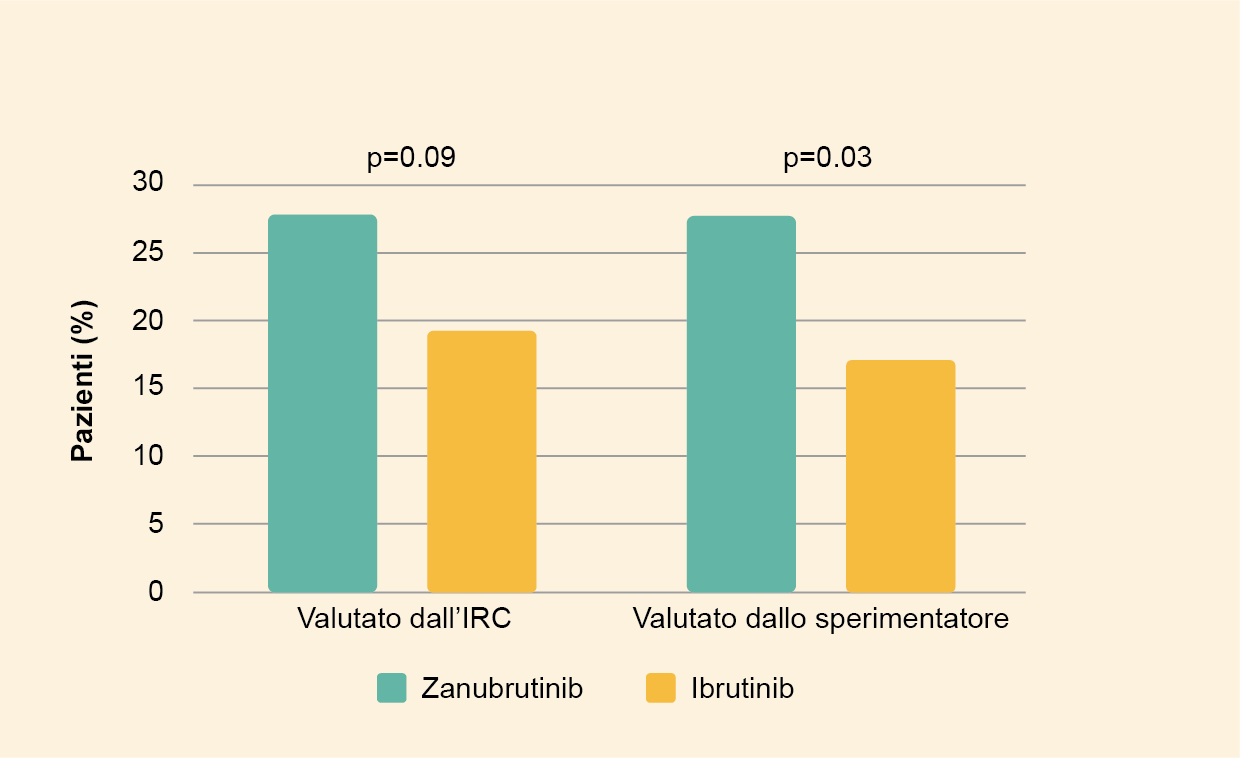
- Dopo un tempo mediano di follow-up di 19,4 mesi, la frequenza delle risposte parziali molto buone (VGPR) è stata superiore tra i pazienti trattati con zanubrutinib rispetto a quelli trattati con ibrutinib (Figura 2).1
Sopravvivenza libera da progressione (PFS) e sopravvivenza complessiva (OS)
- Dopo un tempo mediano di follow-up per la PFS di 18,0 e 18,5 mesi, 15 pazienti (15%) trattati con zanubrutinib e 16 pazienti (16%) trattati con ibrutinib sono peggiorati o deceduti.
- La PFS mediana non è stata raggiunta in nessuno dei bracci di trattamento.
- I tassi di sopravvivenza libera da eventi a 18 mesi erano comparabili: 85% e 84% complessivamente (86% e 82% per i pazienti con malattia R/R).
- Sei (3 R/R; 3 TN) pazienti trattati con zanubrutinib e otto (8 R/R; 0 TN) pazienti trattati con ibrutinib sono deceduti; i tassi OS stimati a 18 mesi sono stati rispettivamente del 97% e del 93%.1
Sicurezza
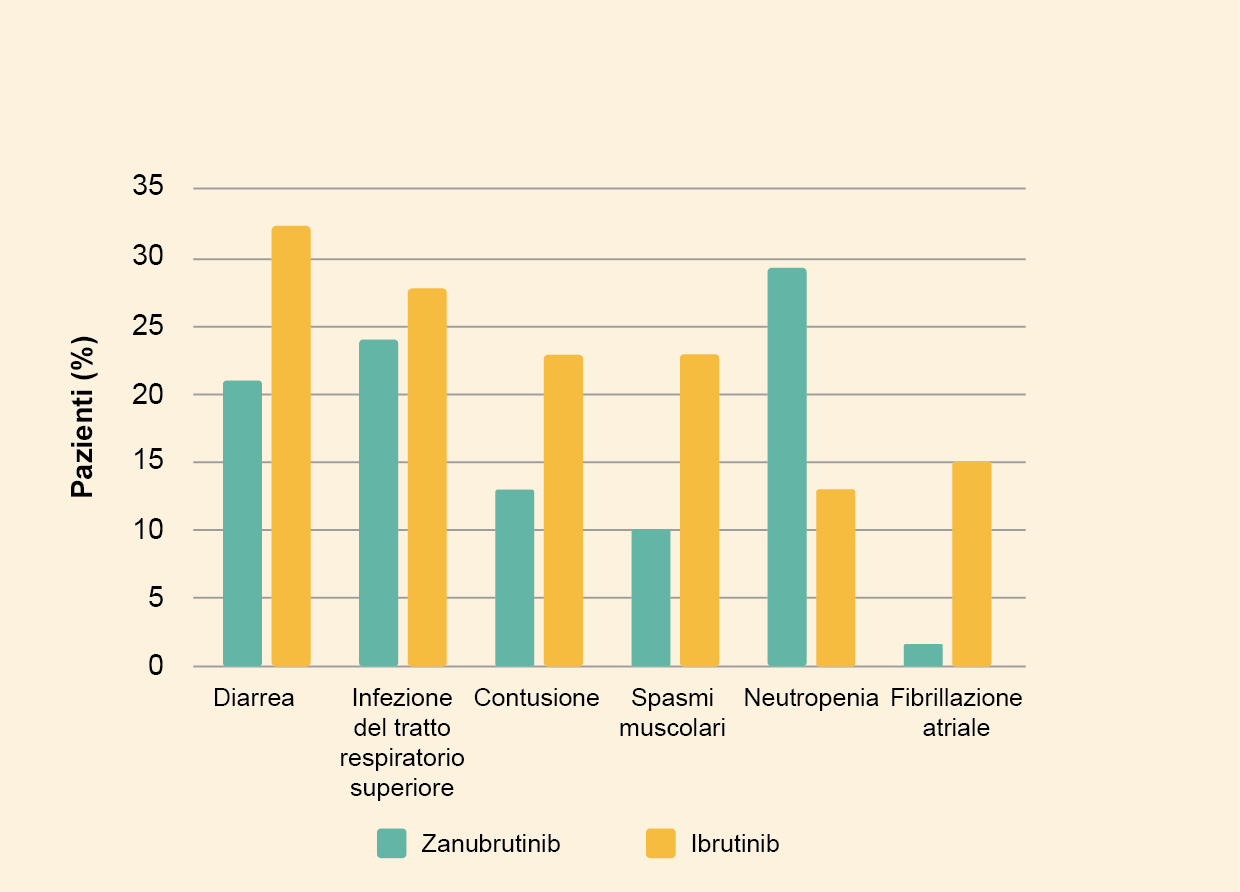
- Gli eventi avversi emergenti dal trattamento (TEAE) più comuni (segnalati in >20% dei pazienti) tra i pazienti che hanno ricevuto zanubrutinib sono stati neutropenia, infezione delle vie respiratorie superiori e diarrea (Figura 3).
- I TEAE più comuni tra i pazienti trattati con ibrutinib sono stati diarrea, infezione delle vie respiratorie superiori, contusione e spasmi muscolari (Figura 3).
- EA di Grado ≥3 sono stati segnalati nel 63% e nel 58% dei pazienti trattati con ibrutinib e zanubrutinib, rispettivamente.
- Ipertensione e polmonite di Grado ≥3 sono state segnalate con un’incidenza superiore del ≥5% tra i pazienti trattati con ibrutinib rispetto ai pazienti trattati con zanubrutinib.
- È stata segnalata neutropenia di Grado ≥3 con un’incidenza superiore del ≥5% tra i pazienti trattati con zanubrutinib.1
Risultati: Coorte 2 (MYD88WT)
Risposte
- In 26 pazienti con MYD88WT confermato, il tasso di risposta complessiva (ORR) è stato dell’81%, con un tasso di risposta maggiore (MRR) del 50,0%, inclusa una VGPR del 27%.2
Sopravvivenza libera da progressione (PFS) e sopravvivenza complessiva (OS)
- A 18 mesi, i tassi stimati di PFS e OS sono stati rispettivamente del 68% e dell’88%, mentre la durata mediana della risposta (DOR) non è stata raggiunta.2
Sicurezza
- Gli EA segnalati più di frequente sono stati diarrea, anemia, contusione, piressia e infezione delle vie respiratorie superiori.
- Soltanto due pazienti hanno interrotto zanubrutinib a causa di EA.2
Riepilogo
- Anche se non statisticamente significativo, è stato osservato un tasso superiore di VGPR secondo la valutazione del comitato di revisione indipendente (IRC) nei pazienti trattati con zanubrutinib rispetto a quelli trattati con ibrutinib (28% rispetto al 19%, rispettivamente) dopo un follow-up mediano di 19,4 mesi nei pazienti con WM MYD88L265P.L265P WM.1
- L’incidenza e la gravità di gran parte delle tossicità associate alla BTK (inclusa fibrillazione atriale) sono state inferiori con zanubrutinib rispetto a ibrutinib.
- Zanubrutinib ha mostrato un’attività antitumorale clinicamente significativa ed è stato ritenuto ben tollerato, con un basso tasso di interruzione dovuto agli EA in pazienti con WM MYD88WT WM.2