iNNOVATE – Ibrutinib
Learn more about the iNNOVATE study and Waldenström’s macroglobulinemia.
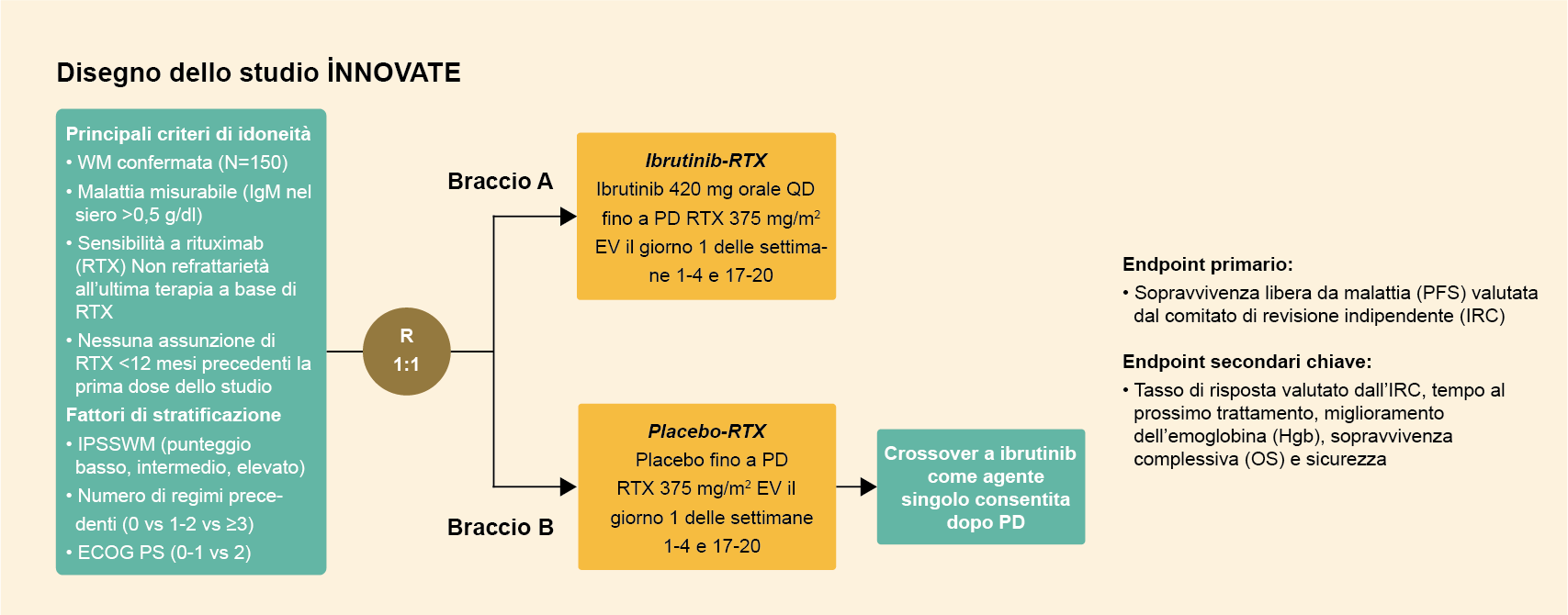
Studio iNNOVATE
- Randomizzazione di 150 pazienti affetti da macroglobulinemia di Waldenström (sia pazienti naïve al trattamento sia pazienti che hanno sviluppato una recidiva della malattia) per ricevere ibrutinib in combinazione con rituximab o rituximab da solo.
- I pazienti sono stati assegnati in modo casuale con un rapporto 1:1 a un gruppo di trattamento per ricevere ibrutinib per via orale (420 mg una volta al giorno) oppure il placebo, fino alla progressione della malattia o fino al manifestarsi di effetti tossici non accettabili.
- I due gruppi hanno ricevuto anche un trattamento prolungato con rituximab per via endovenosa (375 mg per metro quadrato di superficie corporea, con infusioni alle settimane da 1 a 4 e da 17 a 20). 1,2
Risultati
Sopravvivenza libera da progressione (PFS) e sopravvivenza complessiva (OS)
- L’analisi finale nell’ambito dello studio iNNOVATE è stata eseguita dopo un follow-up mediano di 50 mesi. I risultati hanno mostrato una sopravvivenza libera da progressione (PFS) del 68% nel gruppo trattato con terapia combinata rispetto al 25% nel gruppo rituximab-placebo dopo il termine stabilito di 54 mesi.
- La PFS mediana non è stata raggiunta con ibrutinib-rituximab, mentre è stata di 20,3 mesi con placebo–rituximab.
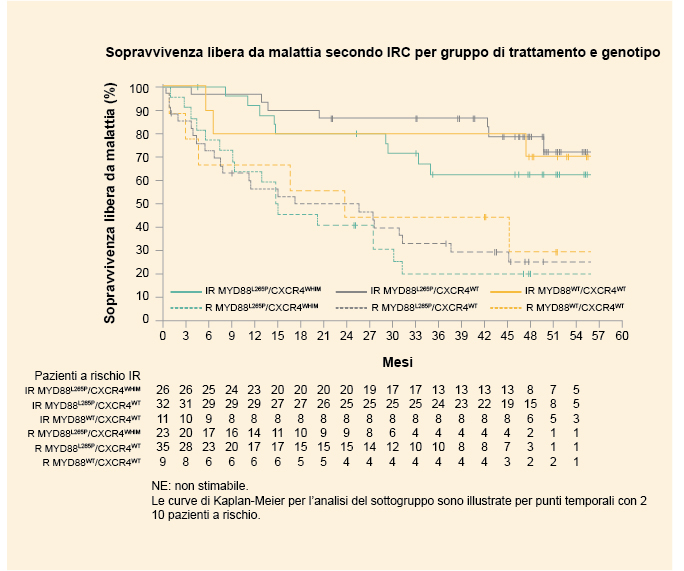
- I pazienti trattati con ibrutinib-rituximab hanno ottenuto un beneficio in termini di PFS indipendentemente dal genotipo (HR (95% CI): MYD88L265P/CXCR4WT, 0.18 (0.08–0.43); MYD88L265P/CXCR4WHIM, 0.27 (0.12–0.62); MYD88WT/CXCR4WT, 0.29 (0.07–1.19)) (Figura 2).
- Il tasso di sopravvivenza complessiva a 54 mesi è stato dell’86% con ibrutinib-rituximab e dell’84% con placebo–rituximab.
Risposte
- Il tasso di risposta maggiore a 60 mesi è stato del 76% nel braccio ibrutinib-rituximab rispetto al 31% per placebo-rituximab (p<0,0001) e il tasso di risposta complessiva è stato del 92% rispetto al 44% (p<0,0001).
- High response rates were observed with combination therapy across genotypes (94% (30/32) in MYD88L265P/CXCR4WT; 100% (26/26) in MYD88L265P/CXCR4WHIM; 82% (9/11) in MYD88WT/CXCR4WT).2
Sicurezza
- Complessivamente, il profilo di sicurezza è risultato coerente con quello del follow-up a 30 mesi. Sono state osservate differenze minime nei tassi di eventi avversi (EA) dopo ulteriori 24 mesi di follow-up e l’incidenza degli EA si è persino ridotta nel corso del tempo.
- Gli EA di Grado 3-4 più comuni sono stati fibrillazione atriale (16%), ipertensione (15%), neutropenia (13%) e anemia (12%).2
Riepilogo
- Con un follow-up fino a 5 anni, ibrutinib-rituximab ha mostrato una superiorità costante nei pazienti affetti da WM, indipendentemente dalle caratteristiche cliniche principali, incluso il genotipo.
- Ibrutinib-rituximab ha mantenuto un profilo di sicurezza gestibile, con nessun nuovo segnale di sicurezza identificato e con incrementi minimi negli EA comuni dopo ulteriori 24 mesi di follow-up.2